Snake Pipe with Hand Ring - Motion Wellness by Xccent Fitness
Enorme nyheter, D-venner: Det nye hurtigvirkende inhalerbare insulin kjent som Afrezza har nettopp fått FDA-godkjenning!
Den tredje gangen er sjarmen for denne nye formuleringen av inhalerbar insulin, den andre til å gjøre det gjennom den amerikanske reguleringsprosessen etter at Pfizers mislyktes Exubera den bedre delen av et tiår siden.
På fredag oppnådde California Biotech Company MannKind Corp endelig godkjenning for sin Afrezza-enhet.

Etter å ha sendt Avrezza tilbake i oktober 2013, har MannKind endelig overbevist FDA om at den er klar til å komme i hendene på voksne med diabetes!
MannKinds toppledere forteller at de jobber for å finne en pharma-partner for å produsere og distribuere Afrezza, og produktet kan bli gjort tilgjengelig så snart januar eller slutten av første kvartal 2015. > I FDAs nyhetsmelding utstedt fredag, sier Dr. Jean-Marc Guettier fra byråets avdeling for metabolisme og endokrinologiprodukter: "Dagens godkjenning utvider alternativene som er tilgjengelige for levering av måltidsinsulin i den overordnede styringen av pasienter med diabetes som krever det å kontrollere blodsukkernivåene. "
Afrezza er et ultrarapidvirkende insulin i pulverform som er utformet som et måltid før måltider for voksne (ennå ikke for barn ) med type 1 eller type 2 diabetes. Den er rettet mot blodsukkerpiker etter måltid, noe som betyr brukt med eksisterende insulinbehandling og ikke ment å være en frittstående insulinbehandling.
Pulverisert insulin administreres via en fløyteformet inhalator som heter Dreamboat, som ble utviklet etter den første FDA-runden og forårsaket forsinkelser fordi byrået ønsket flere kliniske studier ved hjelp av den nye inhalatoren. Pulveret løses umiddelbart når det inhaleres i lungene, og insulinet dumper deretter raskt inn i blodet for å begynne å virke. Afrezza topper innen 12 til 15 minutter og er ute av systemet innen en time, sammenlignet med dagens kortsiktige insuliner som vanligvis tar minst 20 minutter å sparke inn, topp på 2-3 timer, og kan være i systemet for som lenge som fem timer.
Selvfølgelig er den største appellen at det krever ingen nåler, men bare en liten håndholdt inhalator som virkelig ser ut som en fløyte.Dreamboaten er ment å bli kastet vekk etter 15 dager for å forhindre at pulver buildup inni som kunne tette enheten. I motsetning til tradisjonell insulin trenger den ingen kjøling, men holdes heller ved romtemperatur. Hver enkelt-brukskassett vil holde enten 4 eller 8 enheter, og da Afrezza kommer kommersialisert, kan det være en 12-enhetskassett tilgjengelig.
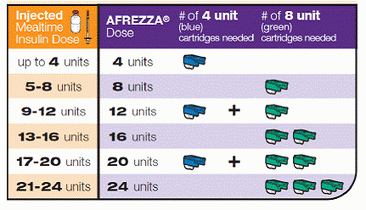
Slik kan du dosere for det, konvertere nåværende insulininjeksjon eller bolus mengder til en Afrezza-vennlig inhalerbar dose:
Personlig ser det ikke ut som mye insulin for å dekke noen av måltidene jeg spiser det krever høyere doser … Jeg ville gå gjennom en hel haug med de små patronene. Så for noen PWDer, kan denne enheten presentere en logistisk utfordring når det gjelder å dosere de beløpene vi trenger …? Men så igjen kan dette være et godt verktøy for å slå ned stædige høyt blodsukker med korreksjonsdosering.
MannKinds president Hakan Edstrom fortalte i en telefonsamtale sent på fredag at selskapet ikke har fullført noen avtaler med potensielle partnere for å produsere og distribuere Afrezza. Men det kommer nær, og i samtaler med en rekke selskaper for å fullføre et partnerskap så snart som mulig.
Kostnadene forblir TBD (mye avhenger av det potensielle partnerskapet), men Edstrom sier at de forventer at prisene skal ligge i samme rekkevidde som det vi pasienter vanligvis betaler nå for insulinpenner i USA.
Denne godkjenningen er en stor utvikling, og det har gått lenge, åtte år siden denne søken begynte av Alfred Mann - mannen som grunnla Minimed før den til slutt ble kjøpt av Medtronic. Vi har fulgt Afrezza-historien i mange år her påMine
- fra den første FDA-arkivdagen da MannKind hadde sin første klare design, til den nyere dekningen om hvordan Afrezza brukes i kunstig bukspyttkjertel kliniske studier.
Den rådgivende komiteen som møtte 1. april i år stemte 13 til 1 at Afrezza var trygg og effektiv nok til godkjenning som behandling for type 1 diabetes, med den ensomme dissenter David Cooke stemte at risikoen oppveide fordelene for typen 1s.Han pekte på den interne FDA-vurderingen som viste at noen pasienter som tok Afrezza, stoppet behandlingen etter å ha utviklet bronkialpasmer, hoste og en nedgang i lungens funksjon. Men ingen av disse bekymringene kom opp under avstemningen på Afrezza for type 2 bruk, og komiteen bestemte seg enstemmig for en 14-0 stemme.
Ved godkjenning av Afrezza har FDA vedlagt en rekke krav til sikkerhet, effektivitet og pasientbruk:Det anbefales ikke for personer med diabetes som røyker, eller for behandling av diabetisk ketoacidose (DKA).

FDA krever en boks advarsel, og anbefaler at noen personer med astma og kronisk obstruktiv lungesykdom (KOL) som har brukt Afrezza, har opplevd akutt bronkospasme. Som følge av dette, bør de med kronisk lungesykdom, astma eller KOL, ikke bruke Afrezza på grunn av denne risikoen. De vanligste bivirkningene forbundet med Afrezza i kliniske studier var hypoglykemi, hoste og hals smerte eller irritasjon.
En del av godkjennelseskravene er en risikovurdering og begrensningsstrategi, som må inneholde en kommunikasjonsplan for å informere helsepersonell om den alvorlige risikoen for akutt bronkospasma forbundet med Afrezza. Det er viktig å sikre at fordelene oppveier de potensielle risikoene ved å bruke Afrezza.
- Andre ettermarkedsstudier kreves på Afrezza, for eksempel: klinisk prøve for å vurdere den potensielle risikoen for lungesvikt ved bruk (denne forsøket vil også vurdere kardiovaskulær risiko og langsiktig effekt av Afrezza på lungefunksjonen); og to farmakokinetiske farmakodynamiske euglykemiske glukose-klemme kliniske studier, en for å karakterisere dose-respons og en for å karakterisere variasjon i individet.
- Edstrom fortalte oss at de planlegger å starte pediatriske forsøk så snart som mulig, noe som realistisk vil begynne en gang i midten av 2015. Det betyr at Afrezza kanskje ikke er godkjent for barn med diabetes til 2017, og at reguleringsprosessen kan variere avhengig av hva ettermarkedsundersøkelsen og bruksopplevelsen viser i mellomtiden.
- Og til tross for FDA-grønt lys, er det ingen garanti for at Afrezza vil se kommersiell suksess, eller at PWDer vil flokkes for å bruke den. Som nevnt har MannKind ennå ikke sikret noen pharma-partnere klar til å selge Afrezza. Men hvis MannKinds inntjeningsanrop i mai er noen indikasjon på hva som kommer snart, kan et potensielt partnerskap ikke være langt unna.
- Fra investorens synspunkt er mange skeptiske basert på det mislykkede Exubera-inhalerte insulin som har formet mye av diskusjonen om Afrezza de siste årene. Det felles Pfizer-Sanofi-produktet ble trukket fra markedet i 2007 etter mer enn et års verdi av under salg, noe som resulterte i en rekordbrytende $ 2. 8 milliarder tap for leverandørene.
- Selvfølgelig hevder MannKind at Afrezza er signifikant forskjellig, hovedsakelig fordi Exubera brukte en klumpete fot lang inhalator og var knyttet til en høyere lungekreftrisiko som Pfizer ikke kunne overvinne.
Vi ser hva D-fellesskapet nå synes med Afrezza, spesielt med alle AP-kliniske forsøksoppmerksomhetene den har hatt nylig. Om det er nok å overbevise massene, er det fortsatt uklart …
Inhale nyheten for nå, og vi vil se hvor lang tid det tar for oss alle å puste ut og forvandle denne spenningen til faktisk salg og utbredt bruk.
Ansvarsfraskrivelse
: Innhold opprettet av Diabetes Mine-teamet. For flere detaljer klikk her.
Ansvarsfraskrivelse
Dette innholdet er opprettet for Diabetes Mine, en forbrukerhelseblogg fokusert på diabetessamfunnet. Innholdet er ikke medisinsk gjennomgått og overholder ikke Healthlines redaksjonelle retningslinjer. For mer informasjon om Healthlines partnerskap med Diabetes Mine, vennligst klikk her.
Inhalert Insulin Afrezza har blitt gitt FDA godkjenning

Godkjente FDA et nytt inhalert insulinprodukt. Afrezza er et ultrarapidvirkende insulin i pulverform, designet som et måltid før diabetikere av type 1.
Inhalert Insulin og Afrezza: Hva du bør vite

DiabetesMin forklarer historien om inhalerbart insulin for diabetes, status for Afrezza og mer.
Inhalert insulin godkjent av FDA: Snakker for OC?




